Liebe Community,
wie hoffen Ihr hattet ein frohes Weihnachtsfest, und konntet im Kreis der Familie tolle Stunden vor dem Aquarium verbringen 
Wir messen in unserem Labor ja nicht nur ICP-OES, sondern führen auch eine Ionenchromatographie (mit zusätzlicher UV-Detektion), eine Leitfähigkeitsmessung, eine photometrische Phosphatbestimmung sowie eine Alkalinitäts-Titration durch. Dabei wird manchmal unterschätzt, dass z.B. die Ionenchromatographie in der Anschaffung einer ICP-OES nicht um viel nachsteht, und zudem die Analyse pro Probe deutlich mehr Zeit in Anspruch nimmt als mit der ICP-OES. Deswegen sollte immer hinterfragt werden, welche Verfahren zur Anwendung kommen, wenn Labors (und die Preise der Analysen) miteinander verglichen werden.
Mit der Ionenchromatographie quantifizieren wir Nitrat, Nitrit, Fluorid, Sulfat, Bromid und Chlorid, und geben Euch auch Auskunft, falls die Probe eine ungewöhnlich hohe Konzentration an Formiat oder Acetat enthält.
Vor allem bei Nitrat machen immer wieder Gerüchte die Runde, dass dieser Parameter in der Probe sehr instabil ist, und daher nicht sinnvoll im Labor gemessen werden kann. - Aber stimmt das? 
Wir haben bisher im Verlauf von 2-3 Wochen Proben-Lagerdauer keine nennenswerte Veränderung des Nitratwerts feststellen können. Hierfür ist vor allem die Steril-Filtration unserer Proben bei der Probenahme verantwortlich, um Stoffwechselaktivitäten (und damit einhergehende Wertveränderungen) zu unterbinden.
Nun haben wir einen etwas „extremeren“ Versuch gemacht, welchen ich mit Euch teilen möchte:
Wir haben 3 „alte“ Proben erneut analysiert, welche nun beinahe ein Jahr lang bei Raumtemperatur gelagert wurden, und haben die Nitrat-Ergebnisse der Originalmessung und der Spätmessung gegenübergestellt:
Probe OC180979, Erstmessung am 10.01.2019, Spätmessung am 21.12.2019, Lagerzeit: 345 Tage
Probe OC181001, Erstmessung am 06.01.2019, Spätmessung am 21.12.2019, Lagerzeit: 349 Tage
Probe OC181107, Erstmessung am 10.01.2019, Spätmessung am 21.12.2019, Lagerzeit: 345 Tage
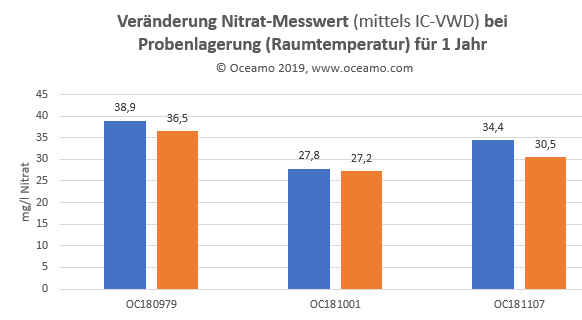
blau: Nitratwert (in mg/l) bei der Erstmessung, Orange: Nitratwert (in mg/l) nach 1 Jahr Lagerdauer der Probe
Wie man gut sehen kann, kommt es selbst bei 1-jähriger Wartezeit zu keinen signifikanten Veränderungen des Nitratwerts - Und so lange muss hoffentlich niemand auf sein Analyseergebnis warten 
Wir wünschen Euch einen guten Rutsch ins neue Jahr!
Viele Grüße,
Christoph
PS.: 2020 wird es wieder mehr Beiträge auf nanoriffe von uns geben, z.B. möchten wir bald Vorbereitungen, Aufbau (und damit verbundene Schwierigkeiten) unseres Schaubeckens hier vorstellen!